Η ΘΡΟΜΒΩΣΗ, ΤΑ ΑΝΤΙΑΙΜΟΠΕΤΑΛΙΑΚΑ ΚΑΙ ΤΑ ΑΝΤΙΦΛΕΓΜΟΝΩΔΗ
Η δημιουργία θρόμβου είναι η αφορμή για την δημιουργία ορισμένων επικινδύνων για τη ζωή καταστάσεων όπως των Οξέων Στεφανιαίων Συνδρόμων (έμφραγμα STEMI και N-STEMI), της οξείας απόφραξης σε Stent όπως και Ισχαιμικών Εγκεφαλικών επεισοδίων.
Μια από τις σπουδαιότερες θεραπείες για τις Καρδιαγγειακές παθήσεις, είναι η αντιαιμοπεταλιακή θεραπεία (μαζί με τις Στατίνες και τις Υγιεινοδιαιτητικές αλλαγές).
Η αντιαιμοπεταλιακή θεραπεία εμποδίζει τη δημιουργία θρόμβων και έτσι μειώνεται ο κίνδυνος για επανεμφάνιση (ή πρώτη εμφάνιση) αθηροθρομβωτικών επεισοδίων, όπως τα εμφράγματα και τα ισχαιμικά εγκεφαλικά.
Ειδικότερα η αντιαιμοπεταλιακή θεραπεία χρειάζεται σε Σταθερή Στεφανιαία Νόσο, σε Οξύ Στεφανιαίο Σύνδρομο, σε τοποθέτηση Stent, μετά από Εγχείρηση Bypass, μετά από Ισχαιμικό Εγκεφαλικό επεισόδιο, σε Αποφρακτική αρτηριοπάθεια των κάτω άκρων κ.λ.π.
Τα αντιαιμοπεταλιακά μειώνουν τα εμφράγματα και τα εγκεφαλικά κατά 25% περίπου σε ασθενείς με αθηρωματική νόσο.
Όμως μερικές φορές δημιουργείται αθηροθρομβωτικό επεισόδιο σε ορισμένους ανθρώπους ενώ είναι υπό θεραπεία με αντιαιμοπεταλιακά φάρμακα.
Περισσότερο από το 10% των ασθενών μετά από έμφραγμα (STEMI/ N-STEMI), παρ’ όλο που είναι σε διπλή αντιαιμοπεταλιακή αγωγή (Ασπιρίνη+Κλοπιδογρέλη), θα ξαναπαρουσιάσει έμφραγμα στον 1ο χρόνο.
Η δημιουργία νέου εμφράγματος παρ’ όλη τη διπλή αιμοπεταλιακή αγωγή αναφέρεται σαν Υπολειπόμενος Κίνδυνος και σχεδόν οι μισές περιπτώσεις από αυτές, εξηγούνται εν μέρει από την μη επαρκή μείωση της συγκολλητικότητας των αιμοπεταλίων από τη αντιαιμοπεταλιακή φαρμακευτική αγωγή (κυρίως από την Κλοπιδογρέλη).
Η μη επαρκής μείωση της συγκολλητικότητας των αιμοπεταλίων ονομάζεται και αντίσταση των αιμοπεταλίων στη δράση των αντιαιμοπεταλιακών φαρμάκων και οφείλεται σε:
Α) Συγχορήγηση άλλων φαρμάκων που εμποδίζουν τον μεταβολισμό και τη δράση τους, π.χ. η μετατροπή της Κλοπιδογρέλης στον ενεργό μεταβολίτη της μπορεί να εμποδιστεί από φάρμακα όπως η Ομεπραζόλη- Losec) και η Εσομεπραζόλη- Nexium.
Β) Μετάλλαξη γονιδίων του ασθενούς που εμποδίζουν τη δημιουργία ενζύμων απαραιτήτων για τη δράση των αντιαιμοπεταλιακών, π.χ. το μεταλλαγμένο γονίδιο 2C19*2 οδηγεί στη δημιουργία ενός αντίστοιχου μη ενεργού ενζύμου 2C19 στο κυτόχρωμα του ήπατος, οπότε η Κλοπιδογρέλη, που είναι προφάρμακο, δεν μπορεί να μετατραπεί από το μη ενεργό ένζυμο, στη δραστική Κλοπιδογρέλη.
Γ) Επιτάχυνση της παραγωγής νέων αιμοπεταλίων
Δ) Μη λήψη των αντιαιμοπεταλιακών φαρμάκων από τον ασθενή.
Ε) Σε μη πλήρη διάλυση του περιβλήματος της αν χορηγείται εντεροδιαλυτή Ασπιρίνη (π.χ. Salospir) κ.λ.π.
Ζ) Σε λήψη ορισμένων αντιφλεγμονωδών φαρμάκων κ.λ.π..
Γενικά αυξημένος κίνδυνος για θρομβώσεις υπάρχει σε: Μεγάλη ηλικία, αν προϋπάρχει παλιό έμφραγμα, σε εκτεταμένη στεφανιαία νόσο, αν πέρασαν λιγότεροι από 12 μήνες από οξύ στεφανιαίο σύνδρομο, σε Σ. Διαβήτη, σε Χρόνια Νεφρική Ανεπάρκεια κ.λ.π..
Αυξημένος κίνδυνος θρόμβωσης σε Stent υπάρχει επιπλέον των ανωτέρω: Αν το Κλάσμα εξωθήσεως είναι κάτω από 40% και σε θέματα που αφορούν το Stent όπως σε μικρή διάμετρο του, σε μεγάλο μήκος του, αν πέρασαν λιγότεροι από 6 μήνες από τοποθέτηση DES κ.λ.π..
Για τον κλινικό υπολογισμό του κινδύνου θρόμβωσης (και σοβαρής αιμορραγίας) αν παραταθεί η διπλή αγωγή σε ασθενείς που τοποθετήθηκε τελευταίας γενιάς DE Stents μπορεί να χρησιμοποιηθεί το DAPT score.
ΛΙΓΑ ΓΙΑ ΤΙΣ ΘΡΟΜΒΩΣΕΙΣ
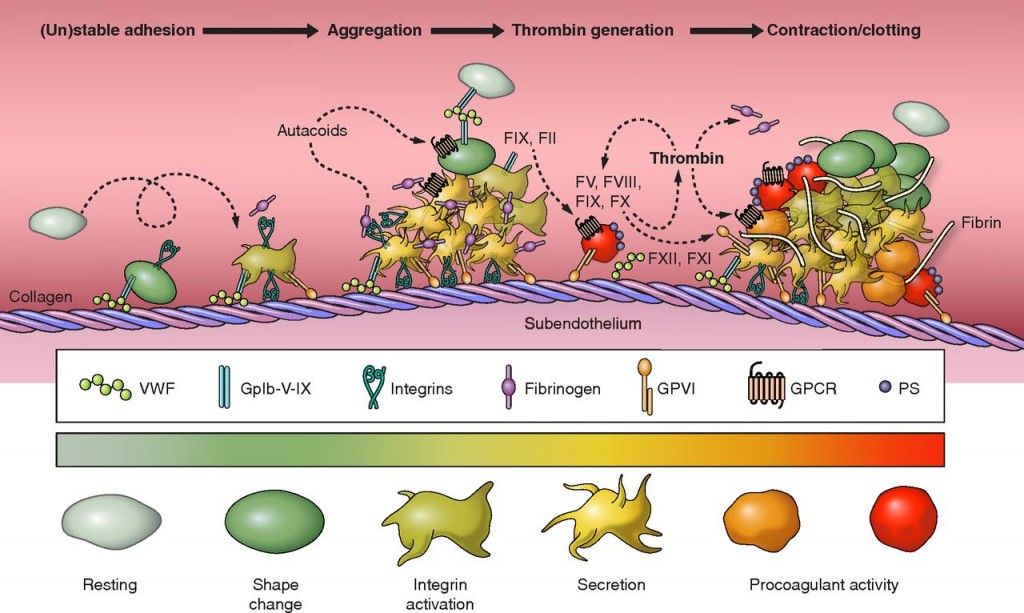
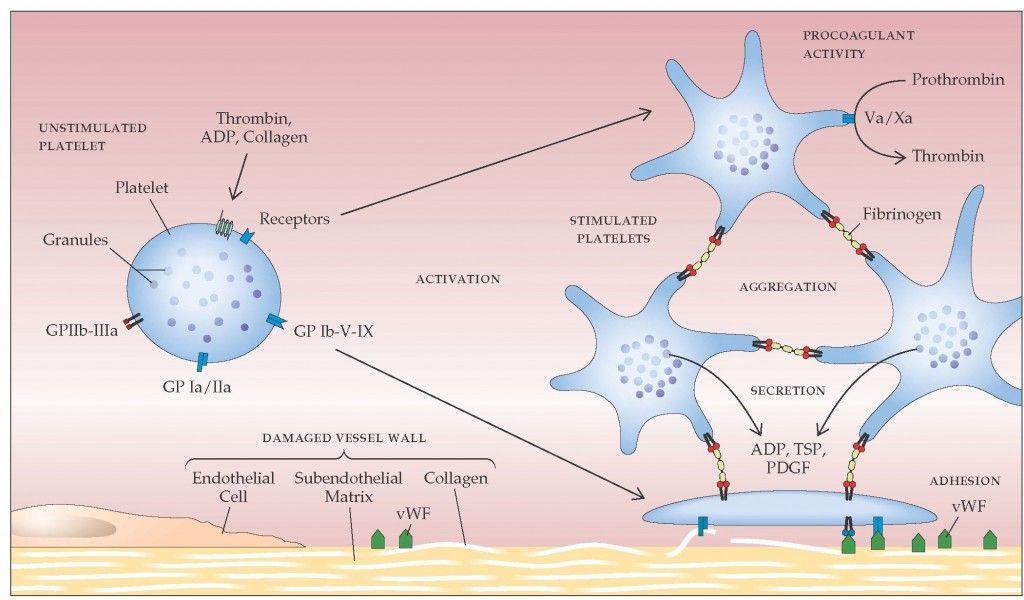
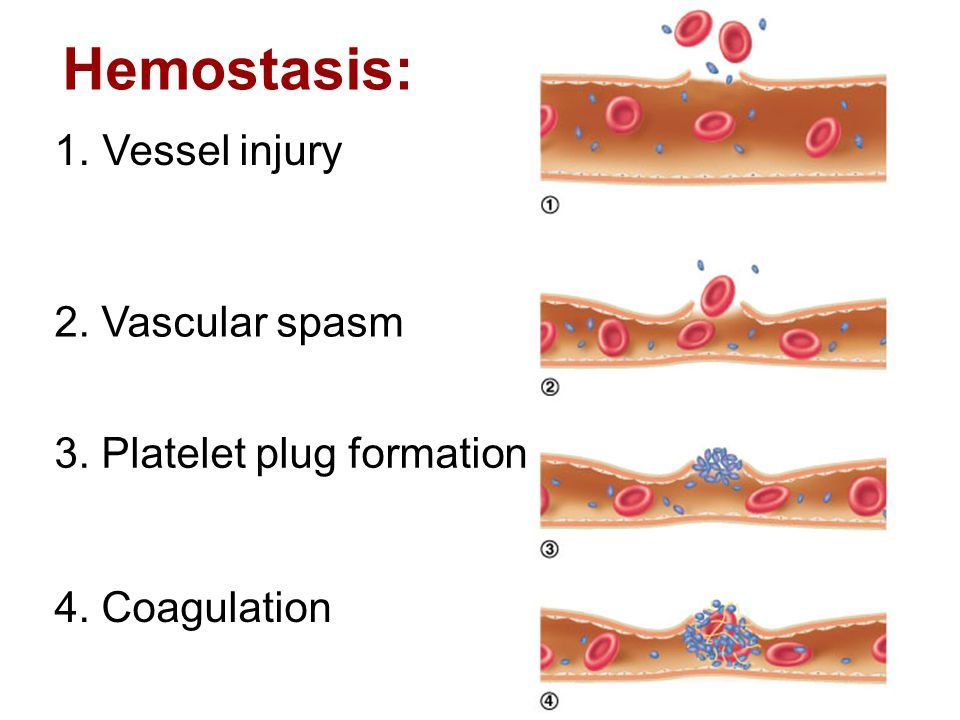
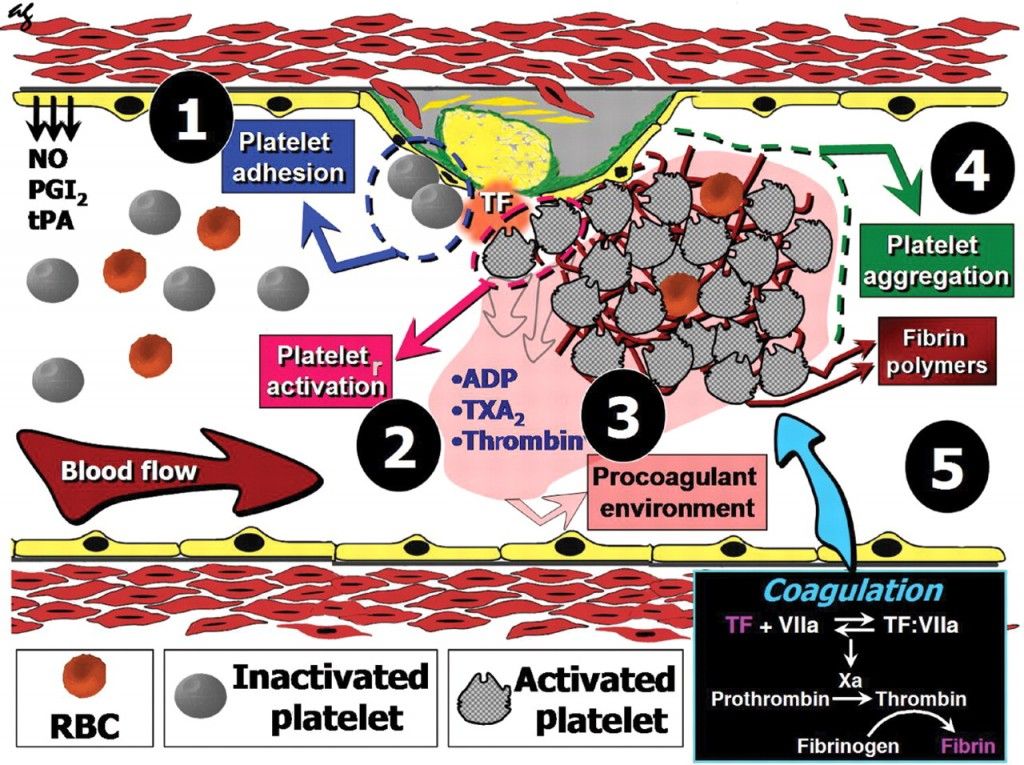
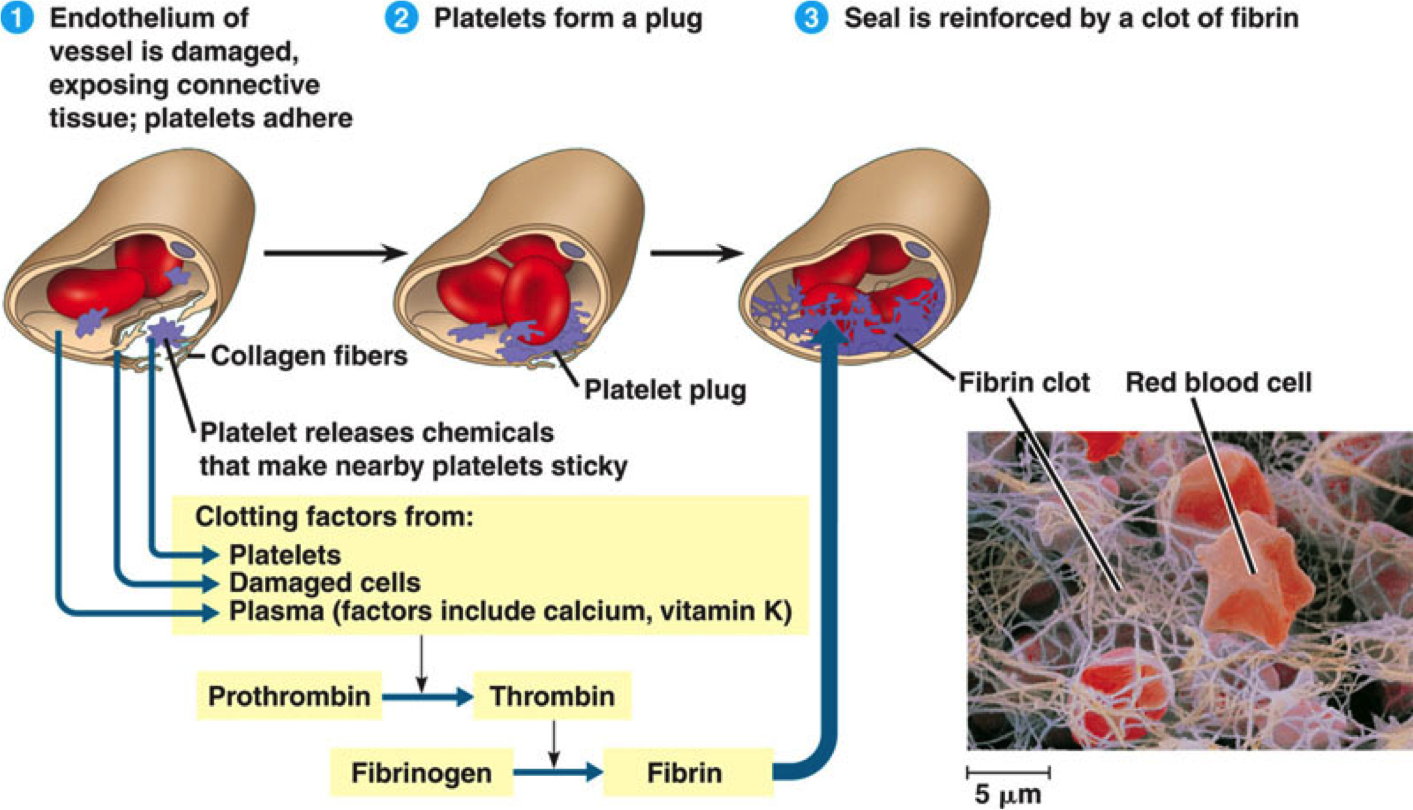
Η δημιουργία του θρόμβου ξεκινά με την προσκόλληση αιμοπεταλίων σε τραυματισμένο ενδοθήλιο στο εσωτερικό των αγγείων, συνεχίζει με την ενεργοποίηση και μετά με την συγκόλληση- αλληλοένωση πολλών αιμοπεταλίων (μέσω μορίων ινοδωγόνου) οπότε δημιουργείται αρχικά ο λευκός αιμοπεταλιακός θρόμβος.
Στη συνέχεια προστίθεται πλέγμα ινώδους και ερυθροκύτταρα οπότε δημιουργείται ο γνωστός τελικός κόκκινος θρόμβος.
Είναι ευνόητο ότι χωρίς την δημιουργία θρόμβων δεν θα ζούσαμε λόγω αιμορραγίας σε περίπτωση τραυματισμού.
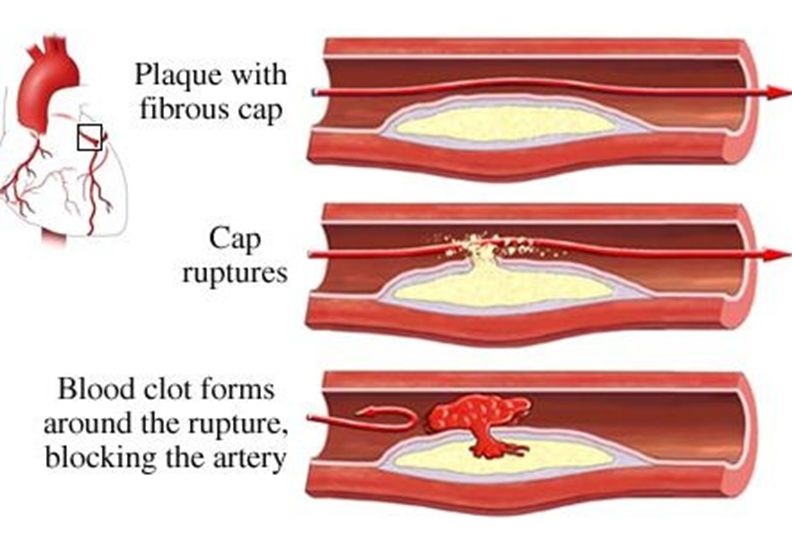
Όμως δυστυχώς οι θρόμβοι δημιουργούνται και σε ρήξη ή διάβρωση του ενδοθηλίου πάνω από αθηροσκληρωτική πλάκα, οπότε αποφράσσεται τελείως ο αυλός της αρτηρίας και το αίμα σταματά να τροφοδοτεί πια την περιοχή μετά την απόφραξη (οπότε έχουμε νέκρωση με Έμφραγμα του Μυοκαρδίου ή με Ισχαιμικό Εγκεφαλικό Επεισόδιο).
Για την αποφυγή των θρομβώσεων που προκαλούν βλάβη, έχουμε τα αντιαιμοπεταλιακά και τα αντιπηκτικά φάρμακα.
Έτσι πρέπει να ισορροπούμε μεταξύ μείωσης των θρομβώσεων (για να μην γίνει Έμφραγμα του Μυοκαρδίου ή Ισχαιμικό Εγκεφαλικό Επεισόδιο) και επικίνδυνων Αιμορραγιών.
Α) Ο ΛΕΥΚΟΣ ΑΙΜΟΠΕΤΑΛΙΑΚΟΣ ΘΡΟΜΒΟΣ ΚΑΙ ΤΑ ΑΝΤΙΑΙΜΟΠΕΤΑΛΙΑΚΑ
Στο εσωτερικό των αρτηριών υπάρχει μια συνεχής ισορροπία θρομβογένεσης / αντιθρόμβωσης που η μεν πρώτη προκαλεί τη δημιουργία, η δε δεύτερη τη διάλυση των αιμοπεταλιακών θρόμβων στα αγγεία.
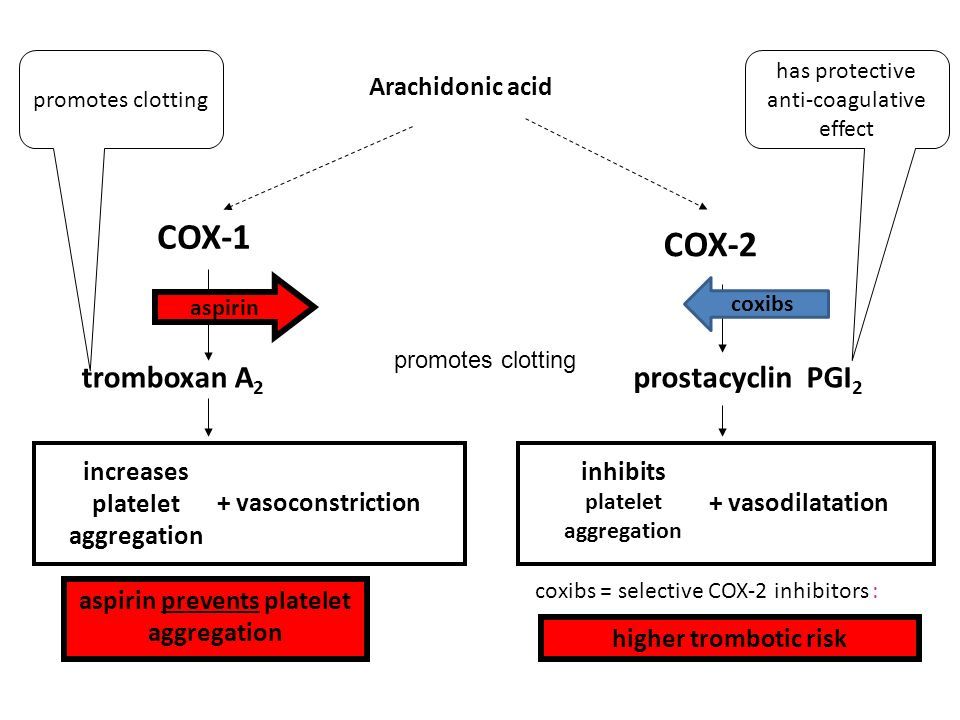
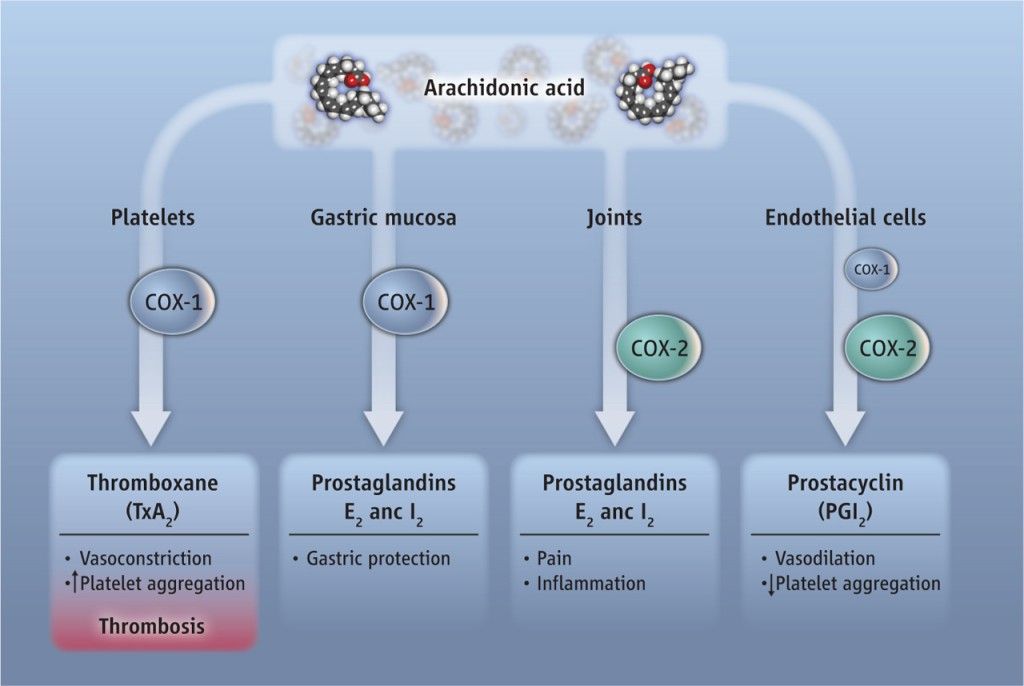
Η θρομβογένεση/ αντιθρόμβωση του αιμοπεταλιακού θρόμβου γίνεται μέσω των αντίθετα δρώντων προσταγλανδινών, Θρομβοξάνης Α2 και Προστακυκλίνης Ι2.
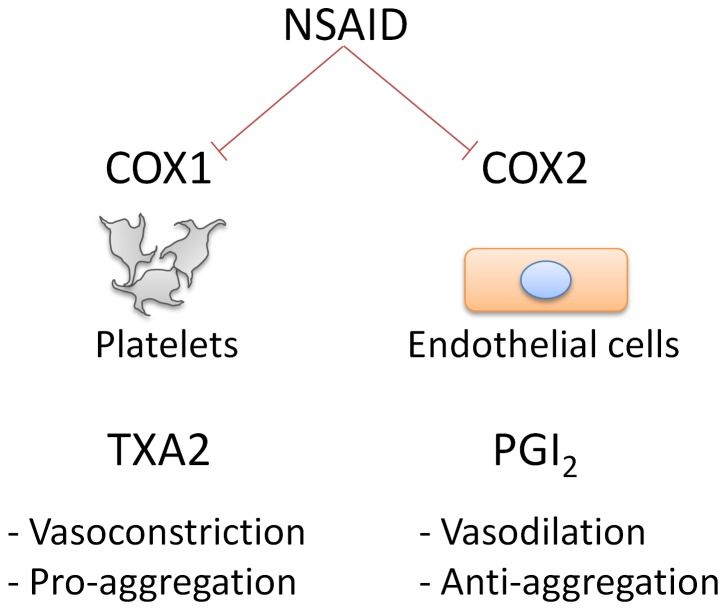
Η Θρομβοξάνη Α2 (ΤΧ-Α2) παράγεται από τα ώριμα αιμοπετάλια, μέσω της κυκλοοξυγενάσης-1 (COX1) και προκαλεί αγγειοσυστολή και δημιουργία θρόμβων (αυξάνει τη συσσώρευση των αιμοπεταλίων).
Η Προστακυκλίνη Ι2 (PG-I2) παράγεται από το υγιές ενδοθήλιο των αγγείων, μέσω της κυκλοοξυγενάσης-2 (COX2) και προκαλεί αγγειοδιαστολή και μείωση των θρομβώσεων (μέσω μείωσης της ενεργοποίησης και συσσώρευσης των αιμοπεταλίων).
Η συγκόλληση των αιμοπεταλίων, για τη δημιουργία του λευκού αιμοπεταλιακού θρόμβου γίνεται μετά από ενεργοποίηση του τελικού υποδοχέα, GP IIb/IIIa στην επιφάνεια τους.
Ένα μόριο ινωδογόνου ενώνεται στους υποδοχείς GP IIb/IIIa δυο διαφορετικών αιμοπεταλίων και τα συγκολλά- ενώνει. Πολλά συγκολλημένα αιμοπετάλια δημιουργούν τον αιμοπεταλιακό θρόμβο.
Η ενεργοποίηση του τελικού υποδοχέα, GP IIb/IIIa γίνεται μετά από διέγερση ορισμένων άλλων υποδοχέων στην επιφάνεια του αιμοπεταλίου με κυριότερους τους υποδοχείς Θρομβοξάνης Α2 (ΤΧΑ2), τους υποδοχείς ADP (Ρ2Υ-12) και τους υποδοχείς θρομβίνης (PAR-1).
ΤΑ ΑΝΤΙΑΙΜΟΠΕΤΑΛΙΑΚΑ
Τα αντιαιμοπεταλιακά φάρμακα εμποδίζουν την συγκόλληση των αιμοπεταλίων δηλαδή τον λευκό αιμοπεταλιακό θρόμβο και χρησιμοποιούνται κυρίως στην Καρδιολογία και στη Νευρολογία.
Τα αντιαιμοπεταλιακά που χρησιμοποιούμε κυρίως σήμερα είναι η Ασπιρίνη και οι ανταγωνιστές των ADP υποδοχέων των αιμοπεταλίων (ή υποδοχέων P2Y- 12).
Υπάρχουν και ανταγωνιστές του τελικά ενεργοποιούμενου υποδοχέα GP IIb/IIIa (Tirofiban, Eptifibatide, Abciximab) αλλά είναι μόνο ενδοφλέβιοι (προς το παρόν) και χρησιμοποιούνται ενδονοσοκομειακά και μόνο σε ορισμένες μόνο περιπτώσεις οξέων στεφανιαίων συνδρόμων και τοποθέτησης stent.
Το Vorapaxar είναι ανταγωνιστής του υποδοχέα της Θρομβίνης των αιμοπεταλίων και έχει βρεθεί ότι συγχορηγούμενο με Ασπιρίνη και Κλοπιδογρέλη σε ανθρώπους με προηγούμενο έμφραγμα, μειώνει κατά 0.5% νέο έμφραγμα ή εγκεφαλικό αλλά και αυξάνει τις σοβαρές αιμορραγίες κατά 1.5%, σε απόλυτες τιμές ανά έτος.
Β) Ο ΚΟΚΚΙΝΟΣ (ΕΡΥΘΡΟΣ) ΘΡΟΜΒΟΣ ΚΑΙ ΤΑ ΑΝΤΙΠΗΚΤΙΚΑ
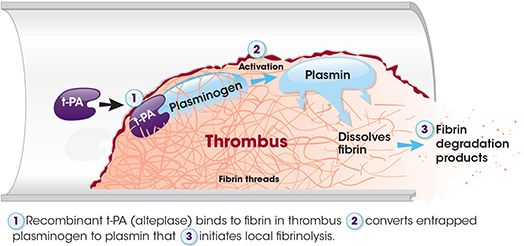
Επίσης στη διαδικασία της θρομβογένεσης / διάλυσης του ΠΛΗΡΟΥΣ- κόκκινου θρόμβου (με το ινώδες και τα ερυθροκύτταρα) συμμετέχει η δημιουργία του ινώδους από την θρομβίνη/ η αυτόματη ενδογενής διάλυση του ινώδους από την πλασμίνη.
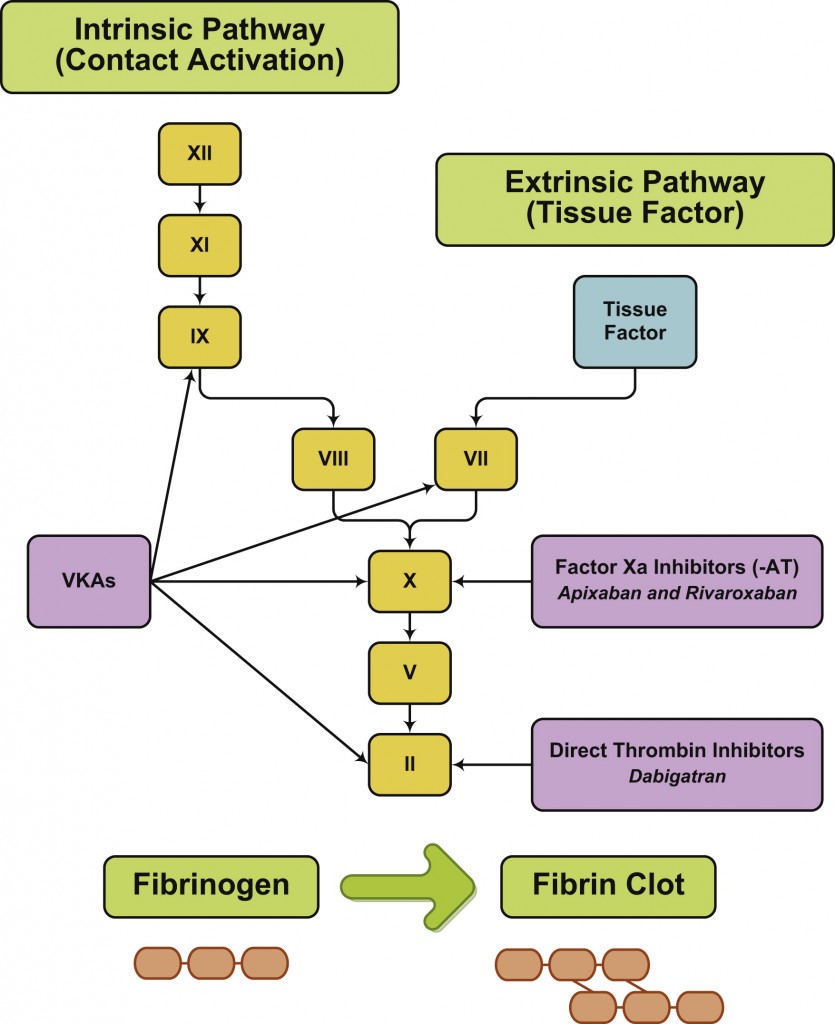
Το Ινώδες είναι το τελικό προϊόν της διαδικασίας της πήξης μέσω των δυο μονοπατιών (εσωτερικού και εξωτερικού) και των παραγόντων της πήξεως. Και τα δυο μονοπάτια καταλήγουν στον παράγοντα Χ και τελικά στο Ινώδες.
Όταν το αίμα εκτεθεί στον Ιστικό παράγοντα που βρίσκεται έξω (εξωτερικό μονοπάτι) από το ενδοθήλιο των αγγείων, ενεργοποιείται ο παράγοντας VII.
Το εσωτερικό μονοπάτι της πήξεως ξεκινά από τραύμα στο ενδοθήλιο (η εσωτερική επικάλυψη του αγγείου), με την ενεργοποίηση του παράγοντα 12 ή F XΙΙ σε F XΙΙa, από την επαφή του με το κολλαγόνο κάτω από το ενδοθήλιο, λόγω εσωτερικού τραύματος του αγγείου, ώστε να παραχθεί τελικά το Ινώδες που θα σχηματίσει τον κόκκινο θρόμβο.
Τα αντιπηκτικά φάρμακα (π.χ. Sintrom, Pradaxa, Xarelto, Eliquis) εμποδίζουν τη δημιουργία του Ινώδους που μαζί με τον λευκό αιμοπεταλιακό θρόμβο σχηματίζουν τον γνωστό μας κόκκινο θρόμβο.
Αυτά χρειάζονται κυρίως σε ανθρώπους με Κολπική Μαρμαρυγή, με τεχνητές βαλβίδες και με εν τω βάθει Θρομβοφλεβίτιδα.
ΤΑ ΑΝΤΙΦΛΕΓΜΟΝΩΔΗ ΦΑΡΜΑΚΑ ΚΑΙ ΟΙ ΘΡΟΜΒΩΣΕΙΣ
Τα αντιφλεγμονώδη εμποδίζουν την δράση των ενζύμων της κυκλο-οξυγενάσης (COX1 και COX2), οπότε μειώνεται η παραγωγή της Προσταγλανδίνης Η2 (PG Η2) που είναι η πρόδρομος ουσία των τελικών προσταγλανδινών PG-E2, PG-I2, PGD2, PGF2α, και TX-A2.
Οι Προσταγλανδίνες είναι ουσίες με δράση παρόμοια των ορμονών και έχουν σχέση με την φλεγμονή αλλά και με άλλες λειτουργίες στον οργανισμό. Παράγονται σε πολλά διαφορετικά σημεία του σώματος και δρουν μόνο τοπικά και βραχυχρόνια.
Τα αντιφλεγμονώδη δρουν μειώνοντας, μέσω της COX 2, την παραγωγή της PG-E2 των λευκών αιμοσφαιρίων που σχετίζεται με πόνο και φλεγμονή.
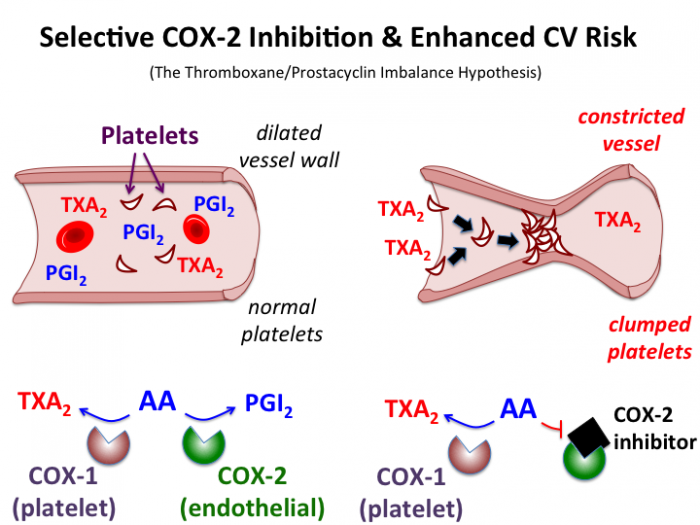
Όσα αντιφλεγμονώδη είναι μόνο (εκλεκτικοί) αναστολείς των υποδοχέων COX2 (Κοξίμπες) ανατρέπουν την ισορροπία θρομβογένεσης / αντιθρόμβωσης προς την πλευρά της θρομβογένεσης.
Αυτό συμβαίνει γιατί μειώνουν την παραγωγή της προστατευτικής προστακυκλίνης PG-I2 από το ενδοθήλιο των αγγείων (μέσω μείωσης της COX2), ενώ αφήνουν ανεπηρέαστη την παραγωγή της βλαβερής θρομβοξάνη ΤΧΑ2 από τα αιμοπετάλια γιατί δεν δρούν στην COX1 (τα ώριμα αιμοπετάλια έχουν μόνο COX1).
Η Δικλοφενάκη και η Ιβοπρουφένη, μειώνουν την COX2 των αγγείων, αλλά ασκούν επιπλέον πολύ μικρή δράση και για πολύ λίγο στην COX1 των αιμοπεταλίων, οπότε μειώνεται ελάχιστα μόνο, η βλαβερή θρομβοξάνη ΤΧΑ2, ενώ μειώνεται πολύ η προστατευτική προστακυκλίνη PGI2 (μέσω μείωσης της COX2) οπότε και αυτά αυξάνουν την θρομβογένεση σε μικρότερο όμως βαθμό από τις Κοξίμπες.
Η Ναπροξένη είναι το ασφαλέστερο (για Καρδιαγγειακά συμβάματα) μη ασπιρινούχο μη κορτικοειδές αντιφλεγμονώδες. Αυτή δεν αυξάνει τα καρδιαγγειακά επεισόδια, γιατί δρα σαν την Ασπιρίνη στα αιμοπετάλια, μειώνοντας όμως προσωρινά την παραγωγή θρομβοξάνης ΤΧΑ2.
Έτσι μειώνει και αυτή την συγκόλληση των αιμοπεταλίων, σε πολύ μικρότερο βαθμό από την Ασπιρίνη που δρα με μη αναστρέψιμο τρόπο στην παραγωγή θρομβοξάνης ΤΧΑ2.
Για την Ασπιρίνη και την Κλοπιδογρέλη και την μη επαρκή αντιαιμοπεταλιακή δράση τους, υπάρχουν άλλα άρθρα στην ιστοσελίδα.