Ο ΚΟΡΩΝΟΪΟΣ SARS-CoV-2 ΚΑΙ Η ΑΝΟΣΟΛΟΓΙΚΗ ΜΝΗΜΗ
Το ανοσοποιητικό μας σύστημα, πέρα από την εξόντωση των εισβολέων μικροοργανισμών, έχει και μια άλλη πολύ σπουδαία αποστολή, να θυμάται τους προηγούμενους εισβολείς και να ανταποκρίνεται άμεσα και ισχυρά για να τους εξοντώσει αν υπάρξει νέα “επίθεση” από τον ίδιο εισβολέα.
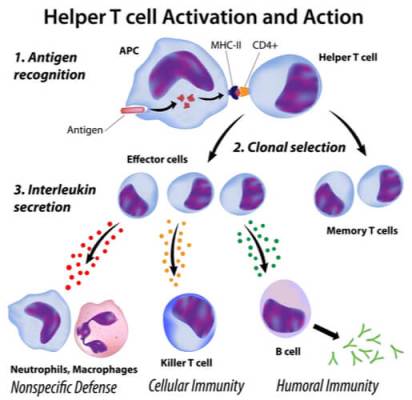
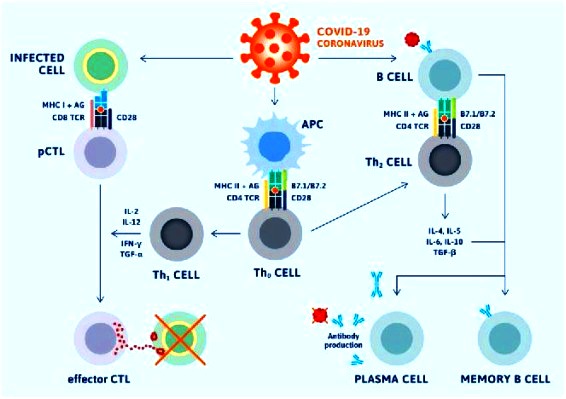
Στην πρώτη εισβολή ενός παθογόνου, τα “παρθένα” (naïve) Λεμφοκύτταρα Τ και Β, διαφοροποιούνται στα αντίστοιχα δραστικά κύτταρα για την εξόντωση του εισβολέα και στα Λεμφοκύτταρα μνήμης Τ και Β, που θα παραμείνουν σε ετοιμότητα ώστε να εξοντώσουν τον ίδιο εισβολέα (αν δεν υπάρχει σημαντική μετάλλαξη του), εφ’ όσον συμβεί νέα “επίθεση” από αυτόν στο μέλλον.
Στην περίπτωση εμβολιασμού τα δραστικά κύτταρα και τα λεμφοκύτταρα μνήμης Τ και Β στρέφονται κατά της πρωτεΐνης ακίδας (spike) του ιού.
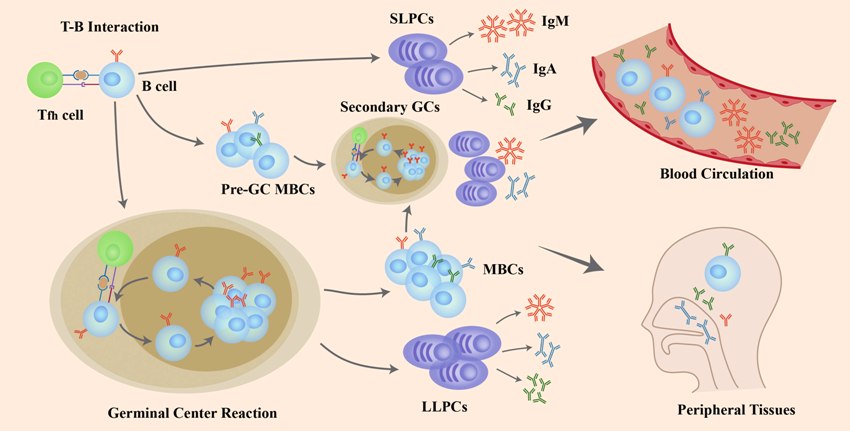
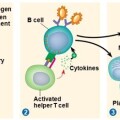
Στην πρώτη εισβολή τα “παρθένα” (naïve) Λεμφοκύτταρα Β διαφοροποιούνται με τη βοήθεια των Tfh λεμφοκυττάρων (Τ follicular helper cells).
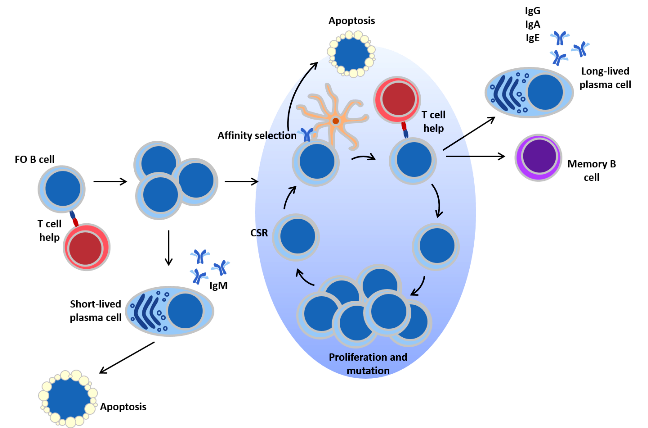
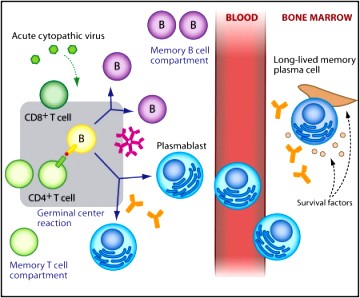
Μετά από αλληλεπίδραση των Β με τα Τ Λεμφοκύτταρα τα Β λεμφοκύτταρα, μετατρέπονται σε βραχείας διάρκειας πλασματοκύτταρα (short-lived plasma cells ή SLPCs), σε Β λεμφοκύτταρα μνήμης μακράς διάρκειας (memory B cells ή MBCs / Αυτά παραμένουν στους λαμφαδένες σε φάση ετοιμότητας) και σε πλασματοκύτταρα μακράς διάρκειας (Long lived plasma cells ή LLPCs) που μεταναστεύουν στο μυελό των οστών, σε “φωλιές” (niches) επιβίωσης, και συνεχίζουν να παράγουν αντισώματα υψηλής ειδικότητας κατά του ίδιου μικροοργανισμού για μήνες ή και χρόνια μετά.
https://www.frontiersin.org/articles/10.3389/fimmu.2022.988536/full
Τα Λεμφοκύτταρα μνήμης Τ και Β, δεν συμμετέχουν κατά την πρώτη εισβολή στην εξουδετέρωση του εισβολέα, παραμένουν κυρίως στους βλεννογόνους που μολύνθηκαν, στους αντίστοιχους λεμφαδένες, στον σπλήνα κλπ. και καιροφυλακτούν για την περίπτωση που μετά από μήνες, χρόνια ή και 10ετίες, ξανα-εισβάλει ακριβώς το ίδιο αντιγόνο (ο ίδιος ιός, το ίδιο μικρόβιο κλπ).
Όσο περιμένουν τα Λεμφοκύτταρα μνήμης Τ και Β αυτo-ανανεώνονται, για να μην εκλείψουν μετά από ορισμένο χρόνο.
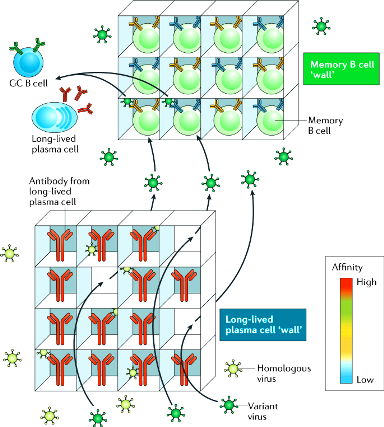
Τα πλασματοκύτταρα LLPCs (δες πιο κάτω) αποτελούν την 1η γραμμή άμυνας σε δεύτερη εισβολή από τον ίδιο μικροοργανισμό (αντιγόνο).
Τα Β κύτταρα μνήμης μακράς διάρκειας που παρέμειναν στους λεμφαδένες και τον σπλήνα ξαναμπαίνουν στον κυτταρικό κύκλο και δημιουργούν τη 2η γραμμή άμυνας.
https://www.nature.com/articles/s41577-019-0244-2
[Υπ’ όψιν ότι έχουν βρεθεί σε μυελό των οστών ειδικά πλασματοκύτταρα μακράς διάρκειας μετά από εμβολιασμό ευλογιάς, περισσότερα από 35 χρόνια μετά την εξάλειψη της.
https://www.frontiersin.org/…/10…/fimmu.2019.01787/full]
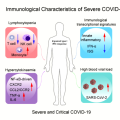
Ειδικότερα για τον ιό SARS-CoV-2, βρέθηκε (μέχρι στιγμής) ότι τα Β λεμφοκύτταρα μνήμης (τα ειδικά για την ακίδα του ιού) ήταν πολύ περισσότερα στους 6 μήνες μετά τη λοίμωξη. Τα δε ειδικά CD4+ και CD8+ T λεμφοκύτταρα είχαν χρόνο ημισείας ζωής περίπου 4 μήνες.
https://science.sciencemag.org/content/early/2021/01/06/science.abf406
https://www.science.org/doi/10.1126/sciimmunol.abl9105
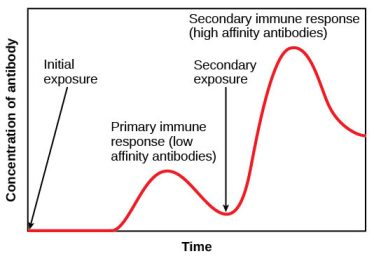
Έτσι η απάντηση του ανοσοποιητικού μας συστήματος σε επόμενη εισβολή του ίδιου μικροοργανισμού, είναι πολύ γρηγορότερη, ισχυρότερη και πιο εξειδικευμένη, συγκριτικά με την πρώτη εισβολή.
Συνεπώς αν ο ιός αυτός συμπεριφέρεται σαν τους άλλους ιούς, ΔΕΝ χρειάζεται να εμβολιαστεί όποιος έχει νοσήσει από Covid 19, αν δεν υπάρξει σημαντική μετάλλαξη του ιού, γιατί τα λεμφοκύτταρα μνήμης Τ και Β είναι έτοιμα να αρχίσουν άμεσα την καταπολέμηση του εισβολέα (ακόμη και αν τα αντισώματα του, IgG, μειωθούν στο ελάχιστο).
Το ότι τα αντισώματα μειώνονται σε λίγο καιρό δεν έχει καμιά σημασία, μειώνονται γιατί εκτέλεσαν την αποστολή τους, την εξόντωση του εισβολέα, και δεν χρειάζεται να συνεχίσει η παραγωγή τους από τα πλασματοκύτταρα.
ΤΑ ΕΜΒΟΛΙΑ ΓΙΑ ΤΟΝ Sars–Cov-2
Στόχος ενός εμβολιασμού είναι η προστασία του εμβολιαζομένου ανθρώπου και επίσης η προστασία του συνόλου του πληθυσμού, με τη διακοπή (ή μεγάλη μείωση) της μετάδοσης του μικροοργανισμού στους ανθρώπους (ανοσία της κοινότητας).
Η προστασία του εμβολιαζομένου αν μολυνθεί από τον συγκεκριμένο μικροοργανισμό κυμαίνεται από 50% (π.χ. γρίπη) ως >90% (π.χ. εμβόλια mRNA), ανάλογα με το εμβόλιο.
Για να διακοπεί η μετάδοση του μικροοργανισμού στον πληθυσμό, συνήθως πρέπει να εμβολιαστεί πάνω από το 70% των κατοίκων, ανάλογα και με την προστασία που προσφέρει το εμβόλιο, και τη μεταδοτικότητα της νόσου.
Τα εμβόλια περιέχουν είτε αντιγόνα του μικροοργανισμού (σε μορφή εξασθενημένου μικροοργανισμού ή σε μορφή τμημάτων του μικροοργανισμού) είτε οδηγίες για την παραγωγή αντιγόνων του μικροοργανισμού από τα ανθρώπινα κύτταρα.
Αυτή τη στιγμή υπάρχουν δυο τύποι εμβολίων κατά του Sars-Cov-2 που χρησιμοποιούν οδηγίες για την παραγωγή αντιγόνου από τα ανθρώπινα κύτταρα (συγκεκριμένα παραγωγή της spike πρωτεΐνης του ιού που χρειάζεται για διείσδυση στα κύτταρα μας).
Και οι δυο τύποι εμβολίου διεγείρουν τα Τ και τα Β λεμφοκύτταρα για την παραγωγή αντισωμάτων από τα Β λεμφοκύτταρα, κατά της spike πρωτεΐνης του ιού.
Το ένα είδος χρησιμοποιεί το mRNA για την παραγωγή από τα κύτταρα μας της spike πρωτεΐνης (εμβόλιο Pfizer-BioNTech, εμβόλιο MODERNA) και προκαλεί αντίδραση του ανοσοποιητικού κατά της spike πρωτεΐνης.
Το άλλο χρησιμοποιεί Αδενοϊό που μεταφέρει το τμήμα του RNA του ιού που παράγει τη spike πρωτεΐνη αγκίστρωσης του SARS-CoV-2, για την παραγωγή από τα κύτταρα μας αυτής της πρωτεΐνης ώστε να προκληθεί αντίδραση του ανοσοποιητικού εναντίον της. (εμβόλιο AstraZeneca, το Ρωσικό εμβόλιο Sputnik V κλπ)
ΛΕΠΤΟΜΕΡΕΙΕΣ ΓΙΑ ΤΑ ΠΛΑΣΜΑΤΟΚΥΤΤΑΡΑ ΜΑΚΡΑΣ ΔΙΑΡΚΕΙΑΣ ΖΩΗΣ (LLPC)
Τα αντισώματα παράγονται για μεγάλα χρονικά διαστήματα, από τα πλασματοκύτταρα μακράς διάρκειας ζωής, μετά από ΜΙΑ ΜΟΝΟ έκθεση σε αντιγόνα ιών ή εμβολίων.
Βρέθηκε ότι ο χρόνος ημίσειας ζωής των αντισωμάτων ήταν: 11 χρόνια για τον Τέτανο, 19 χρόνια για την Διφθερίτιδα, πάνω από 25 χρόνια για την Ηπατίτιδα Α , 50 χρόνια για την Ανεμοβλογιά και εφ’ όρου ζωής για την Ιλαρά και Παρωτίτιδα.
Η διάρκεια της παραγωγής των αντισωμάτων, εξαρτάται από τον αριθμό και τη μακροβιότητα των πλασματοκυττάρων μακράς διάρκειας ζωής.
Τα πλασματοκύτταρα μακράς διάρκειας ζωής (LLPC) είναι τελικώς διαφοροποιημένα κύτταρα που μεταναστεύουν στον μυελό των οστών (στις φωλιές επιβίωσης) και τον λεμφικό ιστό του εντέρου (GALT) και εκκρίνουν συνεχώς αντισώματα για χρόνια, χωρίς να χρειάζεται ξαναδιέγερση τους από το αντιγόνο.
(Όσα LLPC είναι στο μυελό των οστών παράγουν κυρίως αντισώματα IgG και όσα είναι στο έντερο παράγουν κυρίως αντισώματα IgA)
Η μακροβιότητα των LLPC εξαρτάται τόσο από τα γονίδια του αμυντικού συστήματος όσο και από άλλους επιγενετικούς κυρίως παράγοντες. Επιπλέον εξαρτάται και από τη μελλοντική μόλυνση από νέους μικροοργανισμούς, που θα εκτοπίσουν μέρος των ήδη υπαρχόντων LLPC από τις φωλιές επιβίωσης, λόγω προβλήματος χώρου.
https://onlinelibrary.wiley.com/doi/full/10.1111/imcb.12346
Διαφορές στα γονίδια μπορεί να υπάρχουν π.χ. στις πρωτεΐνες MHC που είναι στην επιφάνεια των κυττάρων μας.
[Στην επιφάνεια των κυττάρων μας υπάρχουν πρωτεΐνες (λέγονται MHC) που είναι απαραίτητες ώστε να μπορεί να διαχωρίζει το αμυντικό μας σύστημα, ποια μόρια – αντιγόνα είναι δικά μας και πια είναι ξένα και επίσης αν τα κύτταρα μας είναι φυσιολογικά ή μολυσμένα από ιό κλπ..
Οι MHC είναι 2 κυρίως ειδών, η MHC Ι που εμφανίζεται σε ΟΛΑ σχεδόν τα κύτταρα και η MHC ΙΙ που εμφανίζεται στα κύτταρα των μακροφάγων, των δενδριτικών κυττάρων και των Β λεμφοκυττάρων.]
Οι άλλοι παράγοντες είναι η βοήθεια από άλλα κύτταρα (π.χ. Δενδρικά, Μεγακαρυοκύτταρα, Βασεόφιλα, Ηωσινόφιλα κλπ.) που συνυπάρχουν στις ίδιες “φωλιές” (niches) του μυελού των οστών, το είδος του παθογόνου και του Β λεμφοκυττάρου που τα δημιούργησε κλπ.
[Η μακροβιότητα των πλασματοκυττάρων μακράς διάρκειας ζωής εξαρτάται και από την μεταβολική επάρκεια τους. Αυτή βασίζεται στην ενεργοποίηση των υποδοχέων τους, CD28 από άλλα κύτταρα (π.χ. δενδριτικά κύτταρα) της ίδιας “φωλιάς” στον μυελό των οστών.
https://onlinelibrary.wiley.com/doi/full/10.1111/imcb.12346
https://www.cell.com/cell-reports/pdfExtended/S2211-1247(20)30796-8]
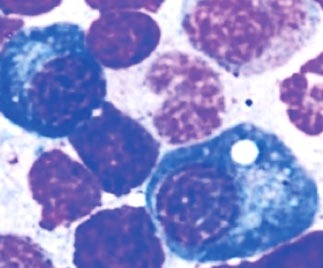
Στην πιο πάνω εικόνα φαίνεται πλασματοκύτταρο μακράς διάρκειας ζωής (κάτω δεξιά, μοιάζει με τηγανητό αυγό) στον μυελό των οστών.
ΕΝΔΕΙΚΤΙΚΗ ΒΙΒΛΙΟΓΡΑΦΙΑ
https://www.science.org/doi/10.1126/sciimmunol.abl9105
https://www.frontiersin.org/articles/10.3389/fimmu.2019.00965/full
https://www.frontiersin.org/articles/10.3389/fimmu.2019.01831/full
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7165522/
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3291529/#:~:text
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC7398916/#CR12
https://www.nejm.org/doi/full/10.1056/NEJMoa066092
https://www.frontiersin.org/articles/10.3389/fimmu.2019.00508/full
https://www.nejm.org/doi/full/10.1056/NEJMe2028079]