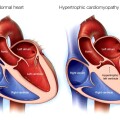
Η ΚΑΤΕΧΟΛΑΜΙΝΕΡΓΙΚΗ ΠΟΛΥΜΟΡΦΗ ΚΟΙΛΙΑΚΗ ΤΑΧΥΚΑΡΔΙΑ- CPVT
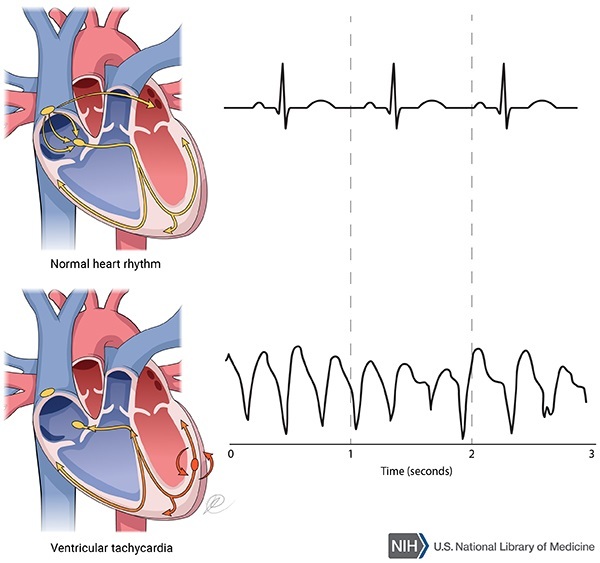
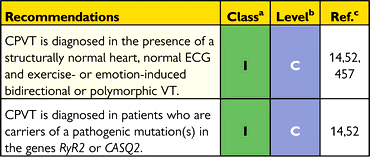
Η κατεχολαμινεργική πολύμορφη κοιλιακή ταχυκαρδία (CPVT) είναι μια σπάνια, κληρονομική γονιδιακή αρρυθμία που μπορεί να προκαλέσει συγκοπτικά επεισόδια και αιφνίδιο καρδιακό θάνατο (SCD) σε σωματική κούραση ή σε συναισθηματική φόρτιση, (από αυξημένες κατεχολαμίνες), κυρίως στις ηλικίες 5 ως 21 ετών.
Η CPVT προκαλεί περίπου το 15% των ξαφνικών ανεξήγητων καρδιακών θανάτων σε νέους και οφείλεται σε διαυλοπάθεια (channelopathy) που προκαλείται από σποραδική ή κληρονομική μετάλλαξη γονιδίων (κυρίως του γονιδίου RYR2 και σπάνια του γονιδίου CASQ2) που αυξάνουν το ενδοκυττάριο Ασβέστιο των καρδιακών μυοκυττάρων στη φάση της διαστολής.
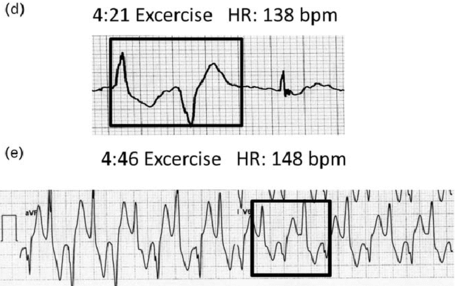
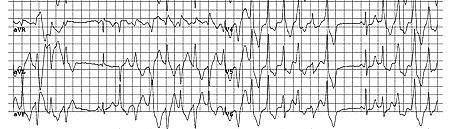
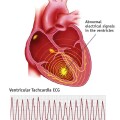
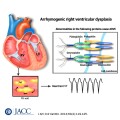
Το συγκοπτικό επεισόδιο ή ο αιφνίδιος καρδιακός θάνατος προκαλείται από μια πολύμορφη κοιλιακή ταχυκαρδία την CPVT που προέρχεται από δυο διαφορετικές εστίες.
Οι εστίες της προέρχονται από τις ίνες του Purkinje και εναλλάσσονται από τη δεξιά και την αριστερή κοιλία διαδοχικά, έτσι σ’ αυτήν ο άξονας του QRS αλλάζει συνεχώς κατά 180 μοίρες.
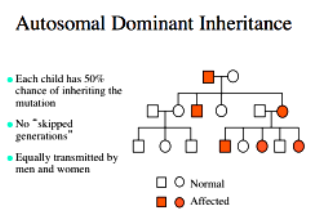
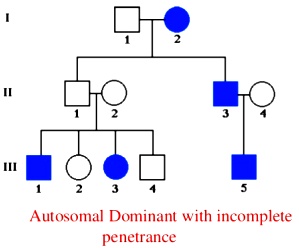
Η CPVT παρουσιάζεται περίπου σε 1 ανά 7.000 παιδιά, κληρονομείται με αυτοσωματική επικρατούσα κληρονομικότητα (με ατελή διεισδυτικότητα, δηλαδή δεν την παρουσιάζουν όλοι όσοι έχουν το μεταλλαγμένο γονίδιο) και δυστυχώς, το ΗΚΓμα ηρεμίας, το Υπερηχοκαρδιαγράφημα όπως και η Καρδιακή Μαγνητική Τομογραφία, είναι φυσιολογικά.
https://www.ahajournals.org/doi/pdf/10.1161/HCG.0000000000000067
Αν η CPVT δεν αναγνωριστεί και αντιμετωπιστεί, θα συμβεί αιφνίδιος καρδιακός θάνατος στο 40% περίπου όσων την έχουν, μέχρι την ηλικία των 40 ετών.
Η ΔΙΑΓΝΩΣΗ ΤΗΣ CPVT
Ο καρδιολόγος θα υποψιαστεί την CPVT αν ο νέος ή το παιδί αναφέρουν συγκοπή ή αίσθημα παλμών σε κούραση ή ψυχική φόρτιση και ταυτόχρονα υπάρχει οικογενειακό ιστορικό ξαφνικού πρόωρου θανάτου.
Επειδή το ΗΚΓφημα συνήθως είναι φυσιολογικό στην ηρεμία, η διάγνωση της βασίζεται σε δοκιμασία κοπώσεως ή σε Holter ή σε δοκιμασία με φόρτιση Αδρεναλίνης, όπου εμφανίζονται πολύμορφες ή από δυο κατευθύνσεις, έκτακτες κοιλιακές συστολές, συχνά σε διδυμία και αν συνεχιστεί το stress, μπορεί να συμβεί η CPVT.
Όμως δυστυχώς και αυτές οι μέθοδοι δεν έχουν σιγουριά 100% για τη διάγνωση της, η ευαισθησία τους είναι περίπου 75%, οπότε μπορεί να χρειαστεί μακροχρόνιο Holter ή και τοποθέτηση υποδορίως Implanted Loop Recorder (ILR) για να φανεί η CPVT.
## Τελικά θα χρειαστεί να διενεργηθεί γονιδιακός έλεγχος για τη σίγουρη διάγνωση της και αν βρεθεί μετάλλαξη του γονιδίου RYR2, θα ακολουθήσει έλεγχος και των άλλων μελών της οικογένειας.
https://www.ahajournals.org/doi/pdf/10.1161/HCG.0000000000000067
Η ΕΝΗΛΙΚΗ ΜΟΡΦΗ ΤΗΣ CPVT ή CPVT 2
Σπάνια (περίπου στο 2%) η CPVT συμβαίνει από μετάλλαξη σε άλλο γονίδιο που σχετίζεται και αυτό με το ενδοκυττάριο Ασβέστιο των καρδιακών μυοκυττάρων, το CASQ2, οπότε ονομάζεται CPVT 2 και συνήθως εκδηλώνεται σε ηλικίες 30 ως 50 ετών, κυρίως σε γυναίκες και έχει λιγότερο κίνδυνο για αιφνίδιο θάνατο.
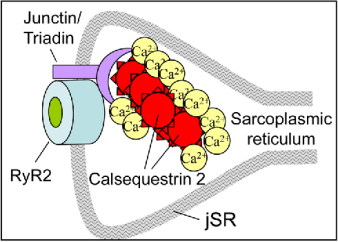
Το γονίδιο CASQ2 δίνει εντολή για την παραγωγή της καρδιακής calsequestrin2 η οποία είναι πρωτεΐνη στο ενδοπλασματικό δίκτυο που συμμετέχει στην αποθήκευση (και μεταφορά) του ενδοκυττάριου Ασβεστίου. Αν η calsequestrin2 είναι μειωμένη ή ελαττωματική έχουμε διαρροή Ασβεστίου προς το κυτταρόπλασμα.
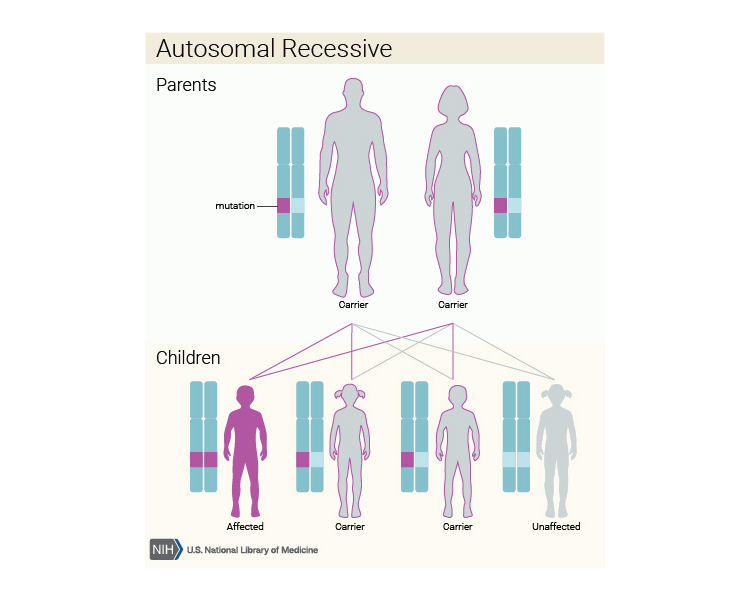
Η CPVT 2 μεταφέρεται με αυτοσωματική υπολειπόμενη κληρονομικότητα δηλαδή πρέπει να υπάρχει η μετάλλαξη και στο γονίδιο από τον πατέρα, και στο γονίδιο από τη μητέρα για να εκδηλωθεί η νόσος στο παιδί.
ΟΙ ΜΕΤΑΛΛΑΞΕΙΣ ΠΟΥ ΑΥΞΑΝΟΥΝ ΤΟ ΕΝΔΟΚΥΤΤΑΡΙΟ ΑΣΒΕΣΤΙΟ
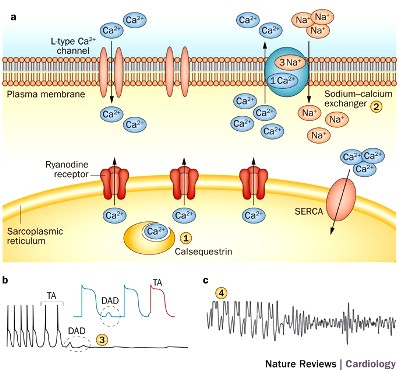
Οι μεταλλάξεις του γονιδίου RYR2 και του γονιδίου CASQ2 προκαλούν αύξηση του ενδοκυτταρίου Ασβεστίου (Ca++) στα μυοκύτταρα της καρδιάς.
Στη “νεανική” CPVT (ονομάζεται και CPVT 1) παρατηρείται μετάλλαξη σποραδική ή κληρονομική του γονιδίου RYR2 (περίπου στο 65% των περιπτώσεων) που δίνει πληροφορίες για την κατασκευή της πρωτεΐνης των καναλιών της Ryanodin 2 (RyR2).
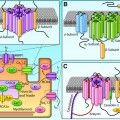
Αυτά τα κανάλια βρίσκονται στο ενδοπλασματικό δίκτυο. Οι μεταλλάξεις του γονιδίου RYR2 (περισσότερες από 150) αλλάζουν τη δομή και λειτουργία της πρωτεΐνης ryanodine receptor 2 και κάνουν τα κανάλια RyR2 να παραμένουν ανοικτά και στη διαστολή (gain-of-function).
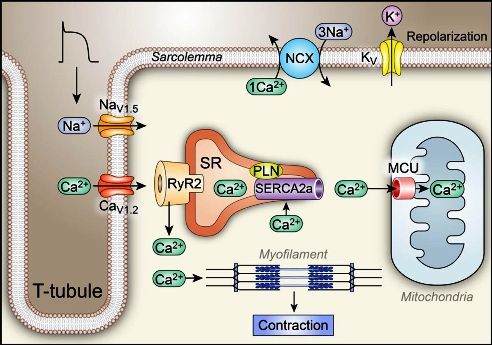
Έτσι βγαίνει περισσότερο Ασβέστιο από το ενδοπλασματικό δίκτυο προς το εσωτερικό του καρδιακού μυοκυττάρου στο κυτταρόπλασμα, κατά τη διαστολή.
https://ghr.nlm.nih.gov/condition/catecholaminergic-polymorphic-ventricular-tachycardia#inheritance
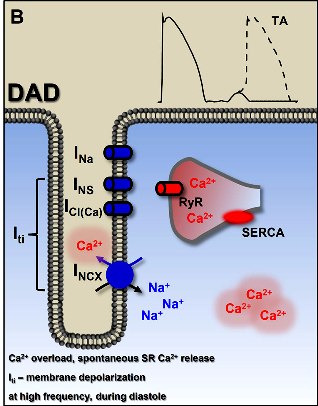
Το επιπλέον Ασβέστιο στη φάση 4 της διαστολής ενεργοποιεί την αντλία Να+/Ca++, για να βγεί το Ασβέστιο έξω από το κύτταρο, έτσι όμως εισέρχεται περισσότερο Νάτριο (έξοδος 1 ιόντος Ca++ και είσοδος 3 ιόντων Na+) στο μυοκύτταρο στην ίδια φάση, οπότε δημιουργείται νέα εκπόλωση.
Η νέα εκπόλωση σε συνδυασμό με αυξημένες κατεχολαμίνες από σωματικό ή ψυχικό stress ευνοεί τη δημιουργία CPVT με μηχανισμούς καθυστερημένων μετ-εκπολώσεων (delayed after depolarizations– DADs).
[Οι κατεχολαμίνες διεγείρουν β αδρενεργικούς υποδοχείς στην επιφάνεια του καρδιακού μυοκυττάρου που δίνουν εντολή για αύξηση του Ασβεστίου σε κάθε σύσπαση, ώστε να δημιουργηθεί ισχυρότερη σύσπαση της καρδιάς.]
https://ghr.nlm.nih.gov/gene/RYR2
ΟΔΗΓΙΕΣ:
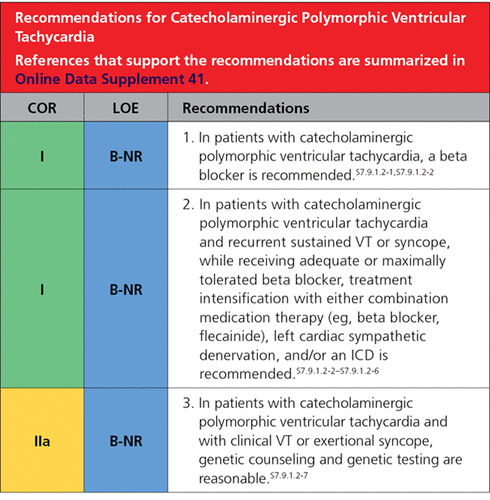
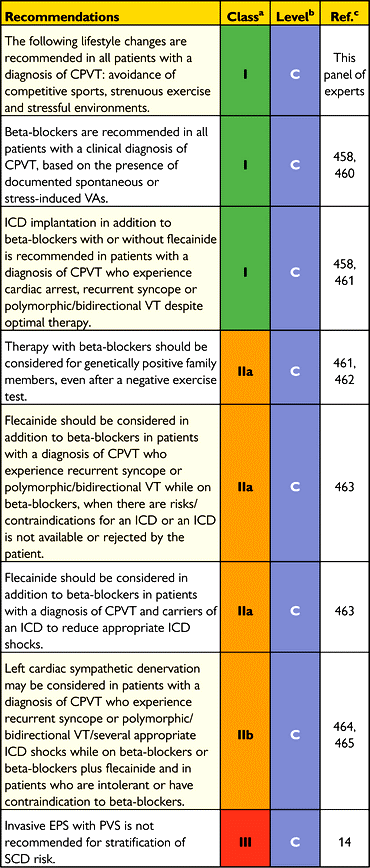
# Σε 1ου βαθμού συγγενείς ανθρώπου με CPVT, συνιστάται διενέργεια δοκιμασίας κοπώσεως και γονιδιακός έλεγχος. Αν βρεθεί να υπάρχει το μεταλλαγμένο γονίδιο τότε χορηγείται β αναστολέας προληπτικά (οδηγία τύπου ΙΙα)
# Δεν συνιστάται ηλεκτροφυσιολογική μελέτη (EPS) για τη διάγνωση της.
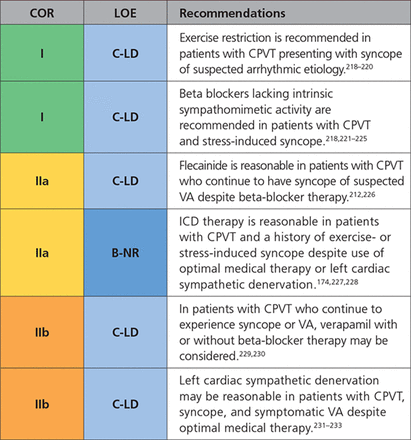
# Σε ασθενείς με CPVT συνιστάται η χορήγηση β- αναστολέα (χωρίς ενδογενή συμπαθομιμηκή δράση) και να αποφεύγεται η σωματική κούραση και οποιαδήποτε κατάσταση ψυχικού stress, ιδίως αν έχει συμβεί συγκοπή στην προσπάθεια. (οδηγία τύπου Ι)
# Σε ασθενείς με CPVT που λαμβάνουν τη μέγιστη ανεκτή δόση β- αναστολέα, προσθέτουμε Flecainide αν συμβεί συγκοπή από πιθανολογούμενη κοιλιακή αρρυθμία ή αν συμβεί επιμένουσα κοιλιακή ταχυκαρδία (οδηγία τύπου Ι).
[Επίσης προστίθεται Flecainide αν συμβαίνουν έκτακτες κοιλιακές συστολές πολύμορφες στη δοκιμασία κοπώσεως παρά τη μέγιστη ανεκτή δόση β- αναστολέα.]
# Αν παρά τη χορήγηση β- αναστολέα και Flecainide, ξανασυμβεί συγκοπή από πιθανολογούμενη κοιλιακή αρρυθμία ή ξανασυμβεί επιμένουσα κοιλιακή ταχυκαρδία, είναι λογικό να τοποθετήσουμε αυτόματο απινιδωτή, ICD (με καθυστερημένη χορήγηση ηλεκτρικής εκκένωσης) με ταυτόχρονη χορήγηση β αναστολέα (οδηγία τύπου ΙΙα).
# Αν ξανασυμβεί συγκοπή από πιθανολογούμενη κοιλιακή αρρυθμία ή ξανασυμβεί επιμένουσα κοιλιακή ταχυκαρδία, παρά τη χρησιμοποίηση ICD και β- αναστολέα (ή αν δεν μπορούν να χρησιμοποιηθούν αυτά), διενεργείται εκλεκτική συμπαθητική απονεύρωση της αριστερής κοιλίας (LCSD ή left cardiac sympathetic denervation) σε εξειδικευμένο κέντρο. (οδηγία ΙΙβ)
Περισσότερες πληροφορίες υπάρχουν στις οδηγίες: 2021 PACES Expert Consensus Statement: https://www.heartrhythmjournal.com/article/S1547-5271(21)01930-5/pdf
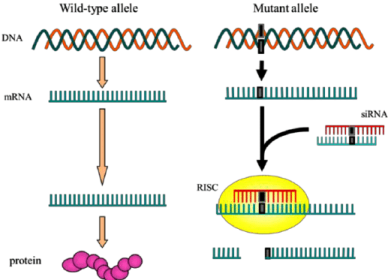
# Επιπλέον δοκιμάζονται πειραματικές θεραπείες για διακοπή της παραγωγής της ελαττωματικής πρωτεΐνης των καναλιών RyR2, π.χ. με siRNA (short-interfering RNA) ώστε να δημιουργούνται μόνο φυσιολογικά κανάλια RyR2 (από το φυσιολογικό γονίδιο που προέρχεται από τον άλλο γονέα).
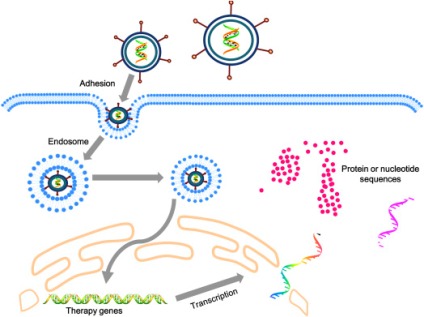
# Άλλες πειραματικές θεραπείες αφορούν τη μεταφορά φυσιολογικού θεραπευτικού γονιδίου (μέσω αδενο-ιού) π.χ. για το γονίδιο CASQ2.
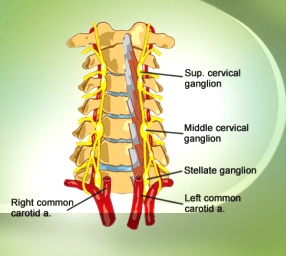
# Ίσως στο μέλλον να φανεί χρήσιμη και η διαδερμική μαγνητική διέγερση (Transcutaneous Magnetic Stimulation ή TCMS), του αριστερού αστεροειδούς γαγγλίου για τη μείωση της συμπαθητικής διέγερσης της καρδιάς.
https://jamanetwork.com/journals/jama/article-abstract/2765760
ΕΝΔΕΙΚΤΙΚΗ ΒΙΒΛΙΟΓΡΑΦΙΑ
https://www.frontiersin.org/articles/10.3389/fphar.2020.00072/full
https://www.mdpi.com/1422-0067/20/21/5304/htm
https://academic.oup.com/eurheartj/article/36/41/2793/2293363
https://www.ahajournals.org/doi/10.1161/CIR.0000000000000549
https://www.ahajournals.org/doi/full/10.1161/CIR.0000000000000499
https://www.nature.com/articles/s41569-019-0266-2
https://www.sciencedirect.com/science/article/pii/S1880427615001349#f0010
https://www.ahajournals.org/doi/10.1161/CIRCULATIONAHA.118.038514
https://academic.oup.com/eurheartj/article/36/41/2793/2293363#108769517